Enfermedad pulmonar obstructiva crónica
| Enfermedad pulmonar obstructiva crónica | ||
|---|---|---|
 Corte de pulmón mostrando cavidades enfisematosos tipo centrolobulillar característico en fumadores. | ||
| Especialidad | neumología | |
| Síntomas | Dificultad para respirar, tos crónica | |
| Causas | Tabaquismo, contaminación del aire, genética | |
| Diagnóstico | Espirometría | |
| Prevención | Dejar de fumar, mejorar la calidad del aire interior y exterior, medidas de control del tabaco | |
| Sinónimos | ||
| EPOC | ||
La enfermedad pulmonar obstructiva crónica (EPOC)[1] es un trastorno pulmonar que se caracteriza por la existencia de una obstrucción de las vías respiratorias generalmente progresiva e irreversible. Se encuentra una mayor incidencia en personas expuestas al humo del tabaco y de leña/carbón, produce como síntoma principal una disminución de la capacidad respiratoria, que avanza lentamente con el paso de los años y ocasiona un deterioro considerable en la calidad de vida de las personas afectadas, pudiendo ocasionar una muerte prematura.[2]
Entre el 20 % y el 25 % de los fumadores desarrolla la enfermedad, pero se desconocen las causas de predisposición al desarrollo, aunque puede que sea un componente multifactorial que incluya elementos ambientales (como susceptibilidad individual).[3]
La causa más común de EPOC es el tabaquismo. Otros factores de riesgo incluyen la contaminación interior y exterior, la exposición a sustancias irritantes ocupacionales como el polvo de los granos y el polvo o vapores de cadmio, y la genética.[4][5] En los países en desarrollo, las fuentes comunes de contaminación del aire interior son el uso de carbón y biomasa como la madera y el estiércol seco como combustible para cocinar y calentar.[6] La mayoría de las personas que viven en ciudades están expuestas a niveles dañinos de contaminación del aire. El diagnóstico se basa en un flujo de aire deficiente medido por espirometría.[4]
La mayoría de los casos de EPOC se pueden prevenir reduciendo la exposición a factores de riesgo como el tabaquismo y los contaminantes interiores y exteriores.[4] Si bien el tratamiento puede retrasar el empeoramiento, no hay evidencia concluyente de que algún medicamento pueda cambiar el deterioro a largo plazo de la función pulmonar. Los tratamientos para la EPOC incluyen dejar de fumar, vacunas, rehabilitación pulmonar, broncodilatadores inhalados y corticosteroides.[4] Algunas personas pueden beneficiarse de la oxigenoterapia a largo plazo, la reducción quirúrgica del volumen pulmonar y el trasplante de pulmón. En aquellos que tienen períodos de empeoramiento agudo, puede ser necesario un mayor uso de medicamentos, antibióticos, corticosteroides y hospitalización.[7]
Definición
[editar]En 2002 el Segundo Consenso Mexicano para el Diagnóstico y Tratamiento de la EPOC lo define como:
El EPOC es una enfermedad caracterizada por limitación al flujo aéreo, la cual no es modificable significativamente y es usualmente progresiva. Esta limitación se asocia con una respuesta inflamatoria anormal de los pulmones y la vía aérea, cuyos factores de riesgo más importantes son la exposición a partículas nocivas y gases, principalmente derivados del consumo de tabaco y exposición a humo de leña.
Según la iniciativa GOLD de 2017, en la Guía para el manejo y prevención de la EPOC:
La Enfermedad Pulmonar Obstructiva Crónica (EPOC) es una enfermedad común, prevenible y tratable que se caracteriza por síntomas respiratorios persistentes y limitación del flujo aéreo que se debe a anomalías de las vías respiratorias y/o alveolares por exposición significativa a partículas o gases nocivos.[8]
Epidemiología
[editar]La prevalencia mundial de la EPOC oscila entre el 5 y el 10 % de la población adulta entre 40 y 80 años. Si consideramos al total de la población, la prevalencia es de aproximadamente el 1 % en todas las edades.[9] La EPOC ha aumentado su prevalencia en las últimas décadas y es 3-4 veces más frecuente en hombres que en mujeres (15 % en fumadores, el 12,8 % en exfumadores y el 4,1 % en no fumadores)[10] dada la mayor prevalencia del tabaquismo en los hombres, aunque esto se espera que cambie en las próximas décadas, ya que el consumo de tabaco en mujeres jóvenes es significativamente mayor al de los hombres jóvenes.[11] Aunque la prevalencia depende en gran parte de la definición fisiológica utilizada, el valor más simple y con mayor sensibilidad es usar la relación FEV1/FVC <0,7 (<70 %).[12] En España se han realizado varios estudios epidemiológicos con base poblacional, obteniendo una prevalencia global de 9,1 % (el 14,3 % en hombres y el 3,9 % en mujeres) de la población de adultos mayores de 40 años.[13][14]
El proyecto Platino, llevado a cabo por la ALAT (Asociación Latinoamericana del Tórax), permitió conocer la prevalencia de la EPOC en cinco países de Iberoamérica (Brasil, Chile, México, Uruguay y Venezuela), variando mucho los porcentajes de un país a otro, entre un 7,8 % en Ciudad de México y un 17 % en Montevideo.[15]
Mortalidad
[editar]La mortalidad global de la EPOC estaba en la sexta posición con 2,2 millones de muertes en 1990, y se prevé una tendencia en ascenso hasta la tercera causa de muerte en 2020.[16] Un estudio realizado en EE. UU. en el período 1971-2000 mostró que el cambio de mayor importancia durante dicho lapso fue el aumento de la mortalidad en mujeres que pasó de 20,1/100 000 en 1980 a 56,7/100 000 en 2000.[17]
En 1998, en España, la EPOC representaba la quinta causa de muerte en los hombres (56,3/100 000 habitantes) y la octava en mujeres (12,3/100 000 habitantes).[18]
Morbilidad
[editar]De forma global, la morbilidad de la EPOC es elevada, aumenta con la edad y es superior en hombres que en mujeres en la actualidad.
Etiología
[editar]La EPOC está fundamentalmente asociada al tabaquismo, sobre todo en países desarrollados. En algunas sociedades muy deprimidas, debido a la exposición a humos tóxicos, puede desarrollarse EPOC. También se da casos, aunque cada vez menos en países desarrollados, de personas que cocinan con fuego de leña en espacios reducidos y mal ventilados.
Factores de riesgo
[editar]En los países desarrollados, el tabaquismo contribuye al 95 % de los casos de EPOC, siendo el factor de riesgo más prevalente.[19] Otros factores comúnmente asociados a una EPOC son:[20]
Factores del huésped
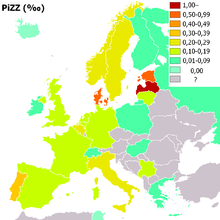
[editar]- Factores genéticos: Existen numerosos informes que afirman que en la patogénesis de la EPOC están o deben estar implicados varios factores genéticos ambientales. Partiendo de la base de que solo un 15-20 % de los fumadores desarrollan la enfermedad, es lógico pensar que la genética debe desempeñar un papel importante en la susceptibilidad individual. No obstante, el estudio Framingham sugiere que, en la población general, los factores genéticos contribuyen muy poco en la pérdida de la función pulmonar,[21] con el flujo espiratorio en primer segundo (FEV1) influenciado principalmente por un locus en el cromosoma 5 brazo q. Un factor genético establecido de la EPOC es la deficiencia de α1-antitripsina (α1-AT) o inhibidor de la proteasa (α1-PI), aunque la deficiencia de α1 (alelo ZZ del gen α1-antitripsina-PiZZ) sucede en menos del 1 % de los casos (ver imagen).[22]
Genes candidatos asociados al desarrollo de EPOC
|
- Dieta: Una ingesta pobre en vitaminas antioxidantes (A, C, E) se ha asociado en algunas ocasiones a un mayor riesgo de EPOC[23][24] y en estudios más recientes se contempla la importancia de la vitamina C y del magnesio.[25] Existe alguna evidencia de que las dietas ricas en aceite de pescado van ligadas a una menor prevalencia de EPOC, aunque estudios similares no confirmaron estos hallazgos. Algunas otras evidencias señalan que una dieta baja en carbohidratos con un mayor aporte de grasas saludables en el requerimiento diario del individuo disminuye la producción de CO2, y podría ser beneficiosa para los pacientes con EPOC. Los flavonoides de las frutas y verduras sí que parecen beneficiosos.[26] Una buena nutrición desde los primeros años de la vida es muy importante y los recién nacidos de bajo peso para su edad gestacional tiene mayor riesgo de desarrollar EPOC en etapas posteriores.
- Atopia e hiperreactividad bronquial: En neumología la llamada hipótesis holandesa que proponía que la atopía y la IgE estaban implicadas en el desarrollo de la EPOC.[27] La EPOC puede tener una mayor reactividad de la vía aérea a la histamina y a la metacolina. Se conoce que la mortalidad por EPOC aumenta con atopia más grave y con hiperreactividad de la vía aérea.[28][29] Un estudio longitudinal indicó una asociación entre eosinoflía y mortalidad por EPOC solo en grupos que habían sufrido ataques de asma.[30]
- Sexo: Varios estudios han encontrado una mayor prevalencia de EPOC en mujeres que en hombres.[31][32] Aunque se discute si las mujeres son más sensibles a los efectos del tabaco, existe evidencia que confirma que las adolescentes jóvenes fumadoras alcanzan una menor función pulmonar,[33] y que para la misma cantidad de exposición al tabaco, el riesgo de tener obstrucción de las vías respiratórias es mayor en mujeres.[34] En los países en desarrollo, las mujeres pueden estar expuestas en mayor grado que los hombres debido a la contaminación ambiental al usar combustibles en la cocina.[35]
Factores ambientales
[editar]- Tabaquismo
- Contaminación atmosférica: La contaminación del aire, especialmente la del dióxido de azufre y la contaminación por partículas respirables (humo negro o partículas de materia <10 μm [PM10]) está asociada a bronquitis crónica simple y a la EPOC.[36] Puede haber interacción entre la contaminación ambiental y el consumo de tabaco. Datos del estudio BOLD no soportan la asociación entre PM2.5 y obstrucción crónica de las vías respiratorias (La prevalencia de Obstrucción de vía aérea no se asoció de forma independiente con PM 2.5), característica de la EPOC.[37]
- Polvo y productos químicos en ambiente laboral: La exposición laboral al polvo (carbón, sílex, cuarzo) a vapores de isocianato y disolventes pueden ser un factor asociado a la aparición de EPOC, actuando con el consumo de tabaco.[38] Se ha estudiado que la exposición al cadmio y la exposición a vapores de soldadura podría estar asociado a la aparición de enfisema.[39]
- Infección: Las infecciones respiratorias durante las primeras etapas de la vida están asociadas a la EPOC en etapas posteriores de la vida.[40][41] Se ha visto que infecciones víricas latentes (como la del adenovirus) pueden causar amplificación de la respuesta inflamatoria en el enfisema y predisponer al desarrollo de EPOC.[42]
- Humo de leña y carbón: las personas que cocinan o calientan el hogar con combustibles de biomasa tienen un gran riesgo de desarrollar EPOC.
Fisiopatología
[editar]En la EPOC se producen distintos fenómenos patológicos en cinco puntos anatómicos, resultando en varias manifestaciones clínicas:[43]
- Bronquitis crónica: inflamación crónica de vía aérea que conduce a hipersecreción mucosa con tos productiva crónica.
- Bronquiolitis obstructiva: inflamación de vía aérea pequeña que provoca fibrosis y remodelado conduciendo a obstrucción de vía aérea.
- Enfisema: debido a destrucción proteolítica con remodelado de bronquiolos y alvéolos.
- Enfermedad vascular pulmonar y cor pulmonale: por destrucción de lecho capilar pulmonar causando hipertensión arterial pulmonar e insuficiencia cardíaca derecha. Esta patología se conoce como cor pulmonale.
- Enfermedad sistémica: en caso de EPOC avanzada hay inflamación extrapulmonar con caquexia y perdida de masa magra con debilidad muscular.[43]
La respuesta inflamatoria exagerada a la inhalación de partículas o gases (fundamentalmente al humo del tabaco), más allá de una respuesta inflamatoria «normal» de protección, es un evento característico de la EPOC que provoca lesiones pulmonares en fumadores susceptibles.[44][45] La lesión de la célula epitelial bronquial y la activación de los macrófagos causan la liberación de los factores quimiotácticos que reclutan a los neutrófilos de la circulación. Los macrófagos y neutrófilos liberan entonces unas proteasas que afectarán a la metaloproteinasas de la matriz (MMP) y a la elastasa de los neutrófilos (NE) provocando alteraciones en el tejido conjuntivo.Una vez secuestrados los neutrófilos se adhieren a la célula endotelial y migran al tracto respiratorio bajo el control de factores quimiotácticos como el leucotrieno B4 o la interleucina (IL)8.
Así mismo, los linfocitos T CD8+ citotóxicos juegan un papel en la cascada inflamatoria. Se ha señalado que la presencia de linfocitos T podría diferenciar entre los fumadores que desarrollan EPOC y aquellos en que no la desarrollan, basado en la relación entre el número de células T, la cantidad de destrucción alveolar y la intensidad de obstrucción al flujo aéreo.[46] Una de las causas que se han descrito para explicar la respuesta inflamatoria amplificada en la EPOC es la colonización de la vía aérea por patógenos bacterianos o víricos.[47] Es posible también que el humo del tabaco dañe la célula epitelial bronquial generando nuevos autoantígenos que estimulan respuesta inflamatoria, llegando a postular que la EPOC fuera una enfermedad autoinmune.[48]
La proteólisis, la fibrosis y el remodelado de las vías aéreas pequeñas son las características prominentes de la patología del enfisema. La célula endotelial vascular, los neumocitos y los mastocitos pueden contribuir también en la patogenia de la EPOC.
Las células y sus mecanismos
[editar]- Macrófagos: La cantidad de macrófagos está muy elevada en las muestras de lavado bronco-alveloar en la EPOC.[49] La activación de estas células se realiza a través del humo del tabaco y otros irritantes inhalados. El número de macrófagos en la vía aérea se corresponde tanto con la extensión de la destrucción del parénquima en el enfisema como con la gravedad de la obstrucción.[50][51] Los pulmones de los fumadores sin EPOC también muestran un número mayor de macrófagos, sin embargo, los macrófagos en los pacientes EPOC están más activados, liberan más proteínas inflamatorias y tiene mayor capacidad elastolítica.[52] En biopsias bronquiales se ha encontrado que los fumadores con EPOC presentan más células expresando la proteína inflamatoria de los macrófagos (MIP-1α).
- Linfocitos T: En pacientes con EPOC, los linfocitos CD8+ (citotóxicos-supresores) aumentan tanto en número como en porcentaje convirtiéndose en el subgrupo de células T dominante. Se ha visto que el incremento de CD8+ está asociado a disminución de la función pulmonar.[53] Estas células podrían contribuir en la fisiopatología de la enfermedad a través de la liberación de grazminas, perforinas y de TNF-α, factores que inducen apoptosis en las células alveolares tipo1. Se desconoce si los CD8+ en el EPOC son de tipo Tc1 (productores de interferón) o del tipo Tc2 (productor de IL-4).
- Neutrófilos
Cuadro clínico
[editar]La EPOC se asocia a dos enfermedades fundamentalmente:
- Enfisema pulmonar: Es el agrandamiento permanente de los bronquiolos terminales, con destrucción de la pared alveolar, pudiendo o no presentarse fibrosis. Esto provoca el colapso de las vías respiratorias. Se suele evidenciar en la clínica por polipnea y taquipnea, pero con disminución del murmullo vesicular a la auscultación y, por aumento del espacio retroesternal en la radiografía lateral izquierda del tórax.[54] El perfil de los pacientes con enfisema (Perfil Pink Puffer) es: astenia, alrededor de 60 años, escasa expectoración, disnea precoz, leve alteración de la difusión de gases, signos radiológicos de hiperinsuflación y bullas, muy baja capacidad de difusión de CO y una resistencia de la vía aérea poco alterada (ocasionalmente elevada). Estos pacientes obtienen poca mejoría clínica con el uso de broncodilatadores y por lo general progresan desfavorablemente con el paso del tiempo.[55]
- Bronquitis crónica: Es una inflamación de los bronquios, que hace que se reduzca el flujo de aire que entra y sale de los pulmones. Paralelamente, hay un aumento de la secreción mucosa que obstruye las vías respiratorias. En términos clínicos, se considera como crónica cuando se aprecia tos y expectoración en la mayor parte de los días durante 3 meses al año, en al menos 2 años consecutivos.[56] El perfil de los pacientes que sufren bronquitis crónica (Perfil Blue bloater) es: sobrepeso, alrededor de 50 años, expectoración abundante, disnea tardía, grave alteración del intercambio de gases, cambios crónicos radiológicos, frecuente aparición de cor pulmonale, disminución leve de la difusión de CO.
Diagnóstico
[editar]
Para el diagnóstico de EPOC se utiliza una prueba llamada espirometría, que mide la capacidad funcional pulmonar. Los sujetos presentan una FEV1 post-broncodilatador menor al 80 % (excepto en el estadio 1, donde VEF1 es mayor o igual al 80 %) y una relación FEV1/FVC menor a 0,70.[57]
Clasificación
[editar]La Global Initiative for Chronic Obstructive Lung Disease [58] ha categorizado los grados de la EPOC en:
| Estadio | Gravedad | FEV1/FVC
Postbroncodilatador |
FEV1 predicho |
|---|---|---|---|
| GOLD 1 | Leve | < 70 % | > 80 % con o sin síntomas crónicos |
| GOLD 2 | Moderada | 50 a 80 % con o sin síntomas crónicos como tos, expectoración, disnea. | |
| GOLD 3 | Grave | 30 a 50% con o sin síntomas crónicos | |
| GOLD 4 | Muy grave | < 30 % o 30 a 50% más insuficiencia respiratoria crónica (PaO2 < 60 mmHg). |
Tratamiento
[editar]La terapia con oxígeno es de uso obligatorio en caso de disminución en la concentración de la saturación de oxígeno, bien sea esta medida con unos gases arteriales o con un oxímetro de pulso.[7]
Los casos de enfermedad crónica se tratan además de los beta 2 agonistas con esteroides inhalados como la beclometasona; además se usa el bromuro de ipratropio, el tiotropio o con glicopirronio bromuro. Se recomienda el uso de esteroides orales superior a catorce días como la prednisona, porque después de este tiempo no hay un efecto demostrado; se han usado esquemas de cinco días de tratamiento oral con buenos resultados los esteroides parenterales como la hidrocortisona o metilprednisolona se indican en el caso de que durante la enfermedad se presente broncoespasmo, de esta manera se reduce la obstrucción al flujo. El uso de teofilina no es contradictorio y no se considera en la mayoría de escenarios. El uso de sulfato de magnesio es controversial, y algunas guías reservan su uso para el asma. Los tratamientos de fisioterapia respiratoria y los ejercicios de rehabilitación pulmonar presentan beneficios en la calidad de vida del paciente[59] y por ello se indica como pilar central en el tratamiento.[7]
Una revisión sistemática de 15 estudios, la mayoría realizados en Asia, particularmente China, y uno en Sudáfrica, encontró evidencia de que la rehabilitación comunitaria genera un impacto positivo. Uno de los casos estuvo centrado en la enfermedad pulmonar obstructiva crónica. Resulta necesaria una evaluación costo-efectividad de las rehabilitaciones que permita evaluar la asignación de los recursos.[60]
Oxigenoterapia
[editar]En general, la administración de oxígeno de forma crónica está indicada en pacientes con EPOC que tienen hipoxemia (PaO2 menor de 55 mm Hg), o una PaO2 entre 55 y 60 mm Hg asociado a hipertensión pulmonar, cor pulmonale, o poliglobulia secundaria (hematocrito >55 %). En estos pacientes la oxigenoterapia continua al menos > de 15 horas al día ha demostrado mejorar la supervivencia.[61] Puede ser necesario bajos flujos de oxígeno dado que en pacientes con EPOC, el control de la respiración está controlado fundamentalmente por los niveles de oxígeno más que por los de carbónico, aumentos de la entrega de oxígeno puede disminuir esta respuesta y causar insuficiencia respiratoria con retención carbónica. Las guías clínicas de la American Thoracic Society sobre EPOC recogen el uso de oxígeno y sus riesgos.[62] Existe un consenso que indica una meta máxima de saturación de oxígeno hasta que la oximetría de pulso marque 92 %, ya que después existe riesgo de hipercapnia inducida por oxígeno.[7]
Tratamiento no farmacológico
[editar]Se recomienda la profilaxis de enfermedad tromboembólica venosa, en agudizaciones que requieran ingreso, y asegurar un adecuado balance hídrico y soporte nutricional.[7]
Calidad de vida
[editar]Los pacientes con EPOC muestran una disminución en la calidad de vida, frente a los valores de referencia para la población en general, en dos componentes principalmente de acuerdo al cuestionario SF36 (Es un cuestionario general que se puede aplicar para medir la calidad de vida relacionada con salud en grupos con diferentes edades, enfermedades o tratamientos) físico y mental. Se ratifica el impacto que tiene la enfermedad en todas las subescalas que componen este constructo, especialmente en el componente físico.[63]
Análisis de asociación genómica multiancestral sobre la función pulmonar
[editar]Una función pulmonar anormal predice mortalidad y es un criterio diagnóstico para la EPOC. [64] Aunque el tabaquismo y otros factores ambientales de riesgo de la EPOC son bien conocidos y se reconoce la susceptibilidad genética, las vías moleculares que subyacen a la EPOC no se conocen del todo. [65] Al igual que con otros rasgos complejos, ha habido una falta de diversidad ancestral en los estudios de asociación de genoma completo (GWAS)[66] de la función pulmonar[67][68][69] . Los estudios multiancestrales mejoran la potencia y la resolución de mapeo fino de los GWAS y aumentan las perspectivas de predicción, prevención, diagnóstico y tratamiento en diversas poblaciones.[66][67][70]
La agregación de variantes genéticas asociadas a la función pulmonar en una puntuación de riesgo genético (GRS) proporciona una herramienta para la predicción de la EPOC.[68] Cuando una GRS comprende muchas variantes, la partición de la GRS según las vías biológicas en las que influyen las variantes podría proporcionar una herramienta para explorar sus consecuencias agregadas a través de diferentes rasgos mediante estudios de asociación de todo el fenotipo (PheWAS). Por tanto, el PheWAS de GRS divididos por vías podría ayudar a comprender las consecuencias de las perturbaciones de vías específicas.[65]
Shrine et al. en 2023[65] mediante el mayor conjunto mundial de estudios genómicos sobre la función pulmonar realizado hasta la fecha:
- Realizaron un metaanálisis GWAS multiancestral de rasgos de la función pulmonar en 588.452 individuos para detectar nuevas señales, mejorar el mapeo fino y estimar la heterogeneidad de los efectos alélicos atribuibles a la ascendencia.
- Comprobaron si las señales de la función pulmonar dependen de la edad o del tabaquismo, y evaluaron su relación con la estatura.
- Investigaron el tipo de célula y la especificidad funcional de señales de asociación pulmón-función
- Señales de mapa fino a través de conjuntos verosímiles informados por anotación, integrando datos funcionales tales como firmas de accesibilidad a la cromatina específicas de células respiratorias
- Aplicaron un marco basado en el consenso para investigar sistemáticamente e identificar genes causales putativos, integrando ocho criterios basados en locus o criterios de similitud
- Desarrollaron y aplicaron una GRS para la relación entre el volumen espiratorio forzado en 1s (FEV1 o VEMS) y la capacidad vital forzada (FVC o CVF) en diferentes ascendencias en el Biobanco de Reino Unido y en estudios de casos y controles de EPOC.
- Aplicaron PheWAS a variantes individuales, GRS para cada rasgo de función pulmonar y GRS dividida por vía.
A través de todas estas aproximaciones, su objetivo fue detectar nuevas señales de la función pulmonar y genes causales putativos, así como proporcionar nuevos conocimientos sobre las vías mecanicistas subyacentes a la función pulmonar, algunas de las cuales podrían ser susceptibles de tratamiento farmacológico.[65]
Se realizaron análisis de asociación de genoma completo (GWAS) de FEV1, FVC, FEV1/FVC y el flujo espiratorio máximo (PEF o FEM) de 49 cohortes. El estudio fue de 588.452 individuos (sus procedencias y el n (número) de cada una se encuentran reflejados en la siguiente figura):

En los análisis específicos de cada cohorte ajustaron por edad, edad al cuadrado, sexo y estatura, teniendo en cuenta la estructura de la población y el parentesco, y luego aplicaron el control genómico mediante el intercepto de regresión de la puntuación de desequilibrio de ligamiento (LD). Tras filtrar y metaanalizar cohortes multiancestrales, se obtuvieron 66,8 millones de variantes en cada uno de los cuatro rasgos de la función pulmonar, con factores de inflación genómica λ de 1,025, 1,022, 0,984 y 0,996 para FEV1, FVC, FEV1/FVC y PEF, respectivamente.
1020 señales para función pulmonar
[editar]
Tras excluir ocho señales asociadas al hábito de fumar y combinar las señales que se localizaban conjuntamente en distintos rasgos (Fig. 1), se identificaron 1.020 señales distintas para la función pulmonar utilizando un umbral estricto de P < 5 × 10-9. De todas estas, 713 no habían sido previamente descritas y estas 1020 señales explican el 33% de la heredabilidad de FEV1/FVC. Para facilitar un mapeo fino, incluyeron poblaciones más grandes y diversas que en anteriores GWAS sobre la función pulmonar.
De los 960 centinelas representados en ≥7 cohortes, 109 señales mostraron heterogeneidad atribuible a la ascendencia, entre ellas, cinco señales mostraron una heterogeneidad significativa relacionada con la ascendencia:
- rs9393688, rs28574670 (LTBP4)
- rs7183859 (THSD4)
- rs59985551 (EFEMP1) y rs78101726 (MECOM)
Examinaron las asociaciones de los SNP asociados a la función pulmonar en cohortes de niños y compararon entre niños y adultos y se vio que tres señales mostraron efectos dependientes de la edad:
- rs7977418 (CCDC91)
- rs34712979 (NPNT)
- rs931794 (HYKK)
Por otra parte, observaron efectos dependientes del tabaquismo para 69 de 1.020 señales. Además, dado que la estatura es un factor determinante del crecimiento pulmonar, compararon las asociaciones entre la estatura y la función pulmonar, sin embargo, no hubo correlación entre los tamaños del efecto estimados para la estatura y la función pulmonar.
Especificidad funcional y de tipo celular
[editar]Posteriormente, evaluaron si esas señales de asociación estaban enriquecidas para características reguladoras o funcionales en tipos celulares específicos:
- Utilizando regresión estratificada de la puntuación de desequilibrio de ligamiento (LD), encontraron enriquecimiento de todas las marcas de histonas analizadas (H3K27ac, H3K9ac, H3K4me3 y H3K4me1) en líneas celulares de pulmón y músculo liso.
- Utilizando GARFIELD (GWAS Analysis of Regulatory or Functional Information Enrichment with LD correction) evaluaron el enriquecimiento de las señales para sitios de hipersensibilidad DNasa l y picos de accesibilidad a la cromatina, y se vio un enriquecimiento en una amplia variedad de tipos celulares.
- Para todos los rasgos, observaron un enriquecimiento para los sitios de inicio de la transcripción, potenciadores débiles, potenciadores y flancos del promotor.
- Para los sitios de unión a factores de transcripción, observaron un patrón de enriquecimiento similar en todos los rasgos de la función pulmonar, con el mayor enriquecimiento observado en las células endoteliales.
- También encontraron un enriquecimiento de los sitios de unión a factores de transcripción en el pulmón en todos los fenotipos y en el bronquio para FEV1/FVC.
Identificación de genes y variantes causales putativos
[editar]Para identificar genes causales putativos, integraron sistemáticamente pruebas ortogonales utilizando ocho criterios basados en locus o similitudes. Se identificaron 559 genes causales putativos que satisfacían al menos dos criterios, de los cuales 135 cumplían al menos tres criterios. Entre los 20 genes apoyados por ≥4 criterios, había:
- Seis genes implicados previamente (TGFB2, NPNT, LTBP4, TNS1, SMAD3 y AP3B1).
- Catorce genes respaldados que no habían sido implicados previamente con seguridad en la función pulmonar (CYTL1, HMCN1, GATA5, ADAMTS10, IGHMBP2, SCMH1, GLI3, ABCA3, STIM1, CFH, FGFR1, LRBA, CLDN18 e IGF2BP2).
Objetivos farmacológicos
[editar]Posteriormente, usando la base de datos Drug Gene Interaction Database, estudiaron 559 genes apoyados por ≥2 criterios y se identificaron 292 fármacos asignados a 55 genes, incluido ITGA2, que codifica la subunidad α 2 de la integrina. La expresión reducida de ITGA2 en el tejido pulmonar asociada con el alelo C de rs12522114 imita la inhibición de ITGA2 inducida por vatelizumab; este alelo se asocia con un mayor FEV1 y FEV1/FVC, lo que indica el potencial de reutilizar vatelizumab para el tratamiento de la EPOC.
Análisis de vías
[editar]Utilizando ConsensusPathDB38, comprobaron el enriquecimiento de las vías biológicas para 559 genes causales respaldados por ≥2 criterios destacando las vías relevantes para el desarrollo, la integridad y la remodelación de los tejidos. Entre ellas se incluyen vías no implicadas anteriormente en los análisis de enriquecimiento de vías para la función pulmonar: la señalización PI3K-Akt, las vías de integrinas, la osificación endocondral, la señalización del calcio, la cardiomiopatía hipertrófica y la cardiomiopatía dilatada, así como las implicadas previamente a través de genes individuales, como la señalización TNF, el citoesqueleto de actina, la señalización AGE-RAGE, la señalización Hedgehog y los cánceres.
GRS multiancestral para FEV1/FVC y EPOC
[editar]Posteriormente, construyeron GRSs multi-ancestrales y ancestrales ponderados por los tamaños del efecto FEV1/FVC y se probó la asociación con FEV1/FVC y EPOC dentro de grupos de individuos de diferentes ancestros en el Biobanco del Reino Unido.
La nueva GRS mejoró la función pulmonar y la predicción de la EPOC en comparación con una GRS anterior basada únicamente en individuos de ascendencia EUR, y la GRS multiancestral superó a la GRS específica de la ascendencia en todas las ascendencias del Biobanco del Reino Unido. Como se observa en la figura 2:

A continuación, probaron la GRS multiancestral en cinco estudios independientes de casos y controles de EPOC y se observaron asociaciones de susceptibilidad a la EPOC más fuertes en los cinco estudios EUR-ancestrales en comparación con una GRS anterior.
PheWAS de las GRS específicas de cada rasgo
[editar]Para estudiar los efectos agregados de las variantes genéticas asociadas a la función pulmonar en una amplia gama de enfermedades y rasgos relevantes para la enfermedad, crearon GRS para: FEV1, FVC, FEV1/FVC y PEF cada una de las cuales comprendía variantes centinela (P < 5 × 10-9) y las probaron en PheWAS. Estos valores de GRS mostraron distintos patrones de asociación con fenotipos respiratorios y no respiratorios, que se encuentran reflejados en la siguiente tabla:
GRS (Puntuación de riesgo genético) Asociación La GRS para un FEV1 más bajo - Mayor riesgo de asma y EPOC
- Antecedentes familiares de bronquitis crónica/enfisema
- Aumento de las exacerbaciones de asma
- Menor edad de inicio de la EPOC
- Mayor estatura de pie y menor estatura sentado
La GRS para un menor FEV1/FVC - Mayor riesgo de EPOC y asma
- Antecedentes familiares de bronquitis crónica/enfisema
- Mayor riesgo de enfisema y de insuficiencia respiratoria
- Menor edad de inicio de la EPOC
- Mayor estatura de pie y sentado
La GRS para una menor FVC - Proteína C reactiva elevada
- Aumento del riesgo de códigos clínicos de asma y EPOC
- Mayor estatura de pie y menor estatura sentado
PheWAS de las GRS repartidas por vías
[editar]Finalmente, llevaron a cabo PheWAS para las GRS ponderadas por FEV1/FVC divididas por cada una de las 29 vías enriquecidas para los 559 genes implicados por ≥2 criterios. La división de los GRS de este modo puso de manifiesto patrones muy diferentes de asociaciones a nivel de todo el fenotipo. Todos demostraron asociación con los códigos clínicos de la EPOC y los antecedentes familiares de bronquitis/enfisema crónico, aunque las asociaciones con otros rasgos variaron y se observan en la siguiente tabla:
GRS (Puntuación de riesgo genético) Asociación La GRS para un menor FEV1/FVC específico de la formación de fibras elásticas - Mayor riesgo de hernia inguinal, hernia abdominal, hernia diafragmática y hernia femoral
- Diverticulosis
- Aumento de la estatura
- Menor riesgo de síndrome del túnel carpiano
- Mayor riesgo de asma
La GRS para un menor FEV1/FVC específico de la señalización PI3K-Akt - Mayor riesgo de asma
- Menor IGF-1
- Descenso de las enzimas hepáticas
- Aumento de eosinófilos
- Menor recuento de linfocitos
La GRS para una menor FEV1/FVC específico de la vía de la cardiomiopatía hipertrófica
- Reducción de las enzimas hepáticas (ALT y GGT)
- Menor nivel de apolipoproteína B
- Menor nivel de LDL e IGF-1
- Aumento de estatura
La GRS para una menor FEV1/FVC específico de la transducción de señales - Mayor riesgo de asma
- Mayor riesgo de enfisema
Conclusión del estudio
[editar]Este estudio multiancestral pone de relieve nuevas variantes, genes y vías causales putativos, algunos de los cuales son el objetivo de compuestos farmacológicos existentes. Estos hallazgos nos acercan a la comprensión de los mecanismos que subyacen a la función pulmonar y la EPOC y servirán de base a experimentos de genómica funcional para confirmar los mecanismos y, en consecuencia, guiar el desarrollo de terapias para el deterioro de la función pulmonar y la EPOC.
Véase también
[editar]Notas
[editar]- ↑ «EPOC o epoc, no Epoc.» Fundéu. Consultado el 5 de marzo de 2015.
- ↑ A. Martin Zurro: Claves diagnósticas en Medicina de Familia, atención al paciente con asma y EPOC en la consulta del médico de familia. Editorial Masson S.A. 2002, ISBN 84-458-1236-X
- ↑ De 2010, 5 De Enero. «EPOC, una enfermedad que afecta al 25% de los fumadores». Infobae. Consultado el 26 de mayo de 2020.
- ↑ a b c d «Informe GOLD 2021».
- ↑ «COPD causes - occupations and subtances». www.hse.gov.uk. Consultado el 6 de noviembre de 2021.
- ↑ Torres-Duque, Carlos A.; García-Rodriguez, María Carmen; González-García, Mauricio (1 de agosto de 2016). «Enfermedad pulmonar obstructiva crónica por humo de leña: ¿un fenotipo diferente o una entidad distinta?». Archivos de Bronconeumología 52 (8): 425-431. ISSN 0300-2896. doi:10.1016/j.arbres.2016.04.004. Consultado el 6 de noviembre de 2021.
- ↑ a b c d e Holden, V; Slack, D; McCurdy, MT; Shah, NG (2017). «Diagnosis and Management of Acute Exacerbation of Chronic Obstructive Pulmonary Disease Confidence interval.». Emergency Medicine Practice 19 (10). PMID 28926214. Consultado el 1 de marzo de 2022.
- ↑ Resumen 2017: Estrategia Global para Diagnóstico, Tratamiento y Prevención de la Enfermedad Pulmonar Obstructica Crónica, Global Initiative for Chronic Obstructive Lung Disease (GOLD) 2017. Disponible en http://goldcopd.org/wp-content/uploads/2016/12/wms-GOLD-2017-Pocket-Guide.pdf
- ↑ «Copia archivada». Archivado desde el original el 27 de febrero de 2015. Consultado el 24 de noviembre de 2014.
- ↑ http://www.archbronconeumol.org/es/datos-epidemiologicos-epoc-espana/articulo/13100985/
- ↑ Pride NB. Chronic obstructive pulmonary disease. Epidemiology, aetiology and natural history. En: Brewis MAL et al editores. Respiratory Medicine. London: Baillière Tindall, 1990.
- ↑ Celli et al. «Population impact of different definitions of airways obstruction.» Eur Respir J. 2003; 22: 268-273.
- ↑ Sobradillo V. et al: Estudio IBEREPOC en España: prevalencia de síntomas respiratorios habituales y de limitación crónica al flujo aéreo. Arch Bronconeumol. 1999; 35: 159-166.
- ↑ Brotons B. Perez J. A. et al: «Prevalencia de la enfermedad pulmonar obstructiva crónica y del asma. Estudio trasversal.» Arch. Bronconeumol. 1994; 30: 149-52.
- ↑ Proyecto Platino
- ↑ Murray et al. MOtality by cause for eight regions of the world:Global Burden of Disease Study.Lancet Murray et al. Alternative projections of mortality and disability by cause 1990-2020:Global Burden of Disease Study.Lancet 1997;349:1498-504
- ↑ Mannino DM et al. Chronic obstructive pulmonary disease surveillance-United Sates, 1971-2000. Repir Care 2002;47:1148-9
- ↑ Centro Nacional de Epidemiología. Instituto de Salud Carlos III. Mortalidad. España y Comunidades Autónomas
- ↑ P.J.Barnes, S.D.Shapiroby R.A.Pauwels. «Enfermedad pulmonar obstructiva crónica: mecanismos moleculares y celulares.» Eur Respir J. (edición española) 2004;5(2):76-95.]
- ↑ Postma, Dirkje S.; Bush, Andrew; Berge, Maarten van den (7 de marzo de 2015). «Risk factors and early origins of chronic obstructive pulmonary disease». The Lancet (en inglés) 385 (9971): 899-909. ISSN 0140-6736. PMID 25123778. doi:10.1016/S0140-6736(14)60446-3. Consultado el 4 de noviembre de 2021.
- ↑ Gottlieb DJ, et al. «Heritability of longitudinal change in lung function. The Framinghan Study.» Am J Crit Care Med. 2001;164:1655-9.
- ↑ Dowson LJ, et al. «Longitudinal changes in physiological, radiological, and health status measurement in alpha(1)-antytripsin deficiency and factors associated with decline.» Am J Respir Crit Care Med 2001;164:1805-9.
- ↑ Britton JR et al Dietary antioxidant vitamin intake and lung function in the general population. Am. J. Respir Crit Care Med 1995;151:1383-7
- ↑ Morabia A. et al. «Vitamin A, cigarette smoking and airway obstruction.» Am Rev Respir Dis. 1989;1312-16.
- ↑ McKeever TM et al. «Propsective study of diet and decline in lung function in a general population.» Am Rev Respir Crit Care Med 2002;165:1299-303.
- ↑ Tabak C et al. «Chronic obstructive pulmonary disease and intake of catechins, flavonols and flavones: the MORGEN Study.» Am Repir Crit Care Med 2001;164:61-4.
- ↑ Orie NGM et al. «The host factor in bronchitis.» In Orie NGM, Sluiter HJ eds. Bronchitis, an international symposium Assen, Netherland:Royal Vangorcum, 1961.
- ↑ Hospers JJ et al. «Histamine airways hyper-responsiveness and mortality from chronic obstructive pulmonary disease:a cohort study.» Lancet 2000;356:1313-17
- ↑ Vestbo J et al. «Airways hiperresponsiveness and COPD mortality.» Thorax 2001;56(Suppl 2) 11-14.
- ↑ Hospers JJ. et al. «Asthma attacks with eosinophilia predictor mortality from chronic obstructive pulmonary disease in general population sample.» Am J Respir Crot Care Med. 1999;160:1869-74.
- ↑ Feinleib M. et al. Trends in COPD morbidity and mortality in the United States. Am. Rev Respir Dis 1989;140:S9-18
- ↑ Prescott E. et al Gender diffrerence in smoking effects on lung function and risk of hospitalization for COPD: results from a Danish longitudinal population study. Eur Respir J 1997;10:822-7
- ↑ Gold DR. et al.Effects of cigarrete smoking on lung function in adolecents boys and girls.N Eng J Med 1996;335:931-7
- ↑ Amaral, André F. S.; Strachan, David P.; Burney, Peter G. J.; Jarvis, Deborah L. (1 de mayo de 2017). «Female Smokers Are at Greater Risk of Airflow Obstruction Than Male Smokers. UK Biobank». American Journal of Respiratory and Critical Care Medicine 195 (9): 1226-1235. ISSN 1073-449X. doi:10.1164/rccm.201608-1545OC. Consultado el 5 de noviembre de 2021.
- ↑ Dennis RJ. et al. Woodsmoke exposure and risk for obstructive airways disease among wome. Chest 1996;109:115-9
- ↑ Abbey DE. et al. «Long-term particulate and other air pollutants and lunng function in nonsmokers.» Am J Respir Crit Care Med 1998;158:289-98.
- ↑ Amaral, Andre F. S.; Burney, Peter G. J.; Patel, Jaymini; Minelli, Cosetta; Mejza, Filip; Mannino, David M.; Seemungal, Terence A. R.; Mahesh, Padukudru Anand et al. (10 de mayo de 2021). «Chronic airflow obstruction and ambient particulate air pollution». Thorax (en inglés). ISSN 0040-6376. PMID 33975927. doi:10.1136/thoraxjnl-2020-216223. Consultado el 5 de noviembre de 2021.
- ↑ Hendrik DJ. et al. Occupational and chronic obstructive pulmonary diasease [COPD]. Thorax 1996;51:947-55
- ↑ Davison AG. et al. Cadmium fume inhalation and emphysema. Lancet 1988;1:663-7
- ↑ Barker DJ et al. The intrauterine an early postnatal origins of cardiovascular disease and chronic bronchitis. J Epidemiol Community Health 1989;237-40
- ↑ Stracha DP. et al Chest illness in infancy and chronic respiratory disease in later life:an analisys by month of birth. Int Epidemiol 1994;23:1060-8
- ↑ Retamales I. et al. Amplification of inflammation in emphysema and its association with latent adenoviral infection. Am J Repir Crit Med 2001;164:469-73
- ↑ a b T Hansel and Peter J. Barnes. Atlas de la Enfermedad Pulmonar Obstructiva Crónica2005. 1;en Parthenon Publishing
- ↑ Cosio el al. Nuevas perspectivas terapéuticas farmacológicas en el manejo de la EPOC. Arch Bronconeumol 2007;43 Supl 4:27-35
- ↑ Hogg JC et al. The nature of small airways obstruction in chronic obstructive disaese. N Engl J Med 2004;350:2654-53
- ↑ Saetta M et al. CD8+ T-lymphocytes in peripheral airways of smokers with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1998;157:882-6
- ↑ Retamales et al. Amplificatioon of inflamamtion in emphysema and its association with latent adenoviral infection. Am J Respir Crit Care Med 2000;164:496-73
- ↑ Agusti A. et al. Hypotesis:does COPD have an autoinmune component.Thorax 2003;58:832-4
- ↑ Pesci et al. Inflammatory cells and mediators in bronchial lavage of patients with chornic obstructive pulmonary disease. Eur Respir J 1998;12:380-6
- ↑ Finkelstein, R; Fraser, R S; Ghezzo, H; Cosio, M G (1 de noviembre de 1995). «Alveolar inflammation and its relation to emphysema in smokers.». American Journal of Respiratory and Critical Care Medicine 152 (5): 1666-1672. ISSN 1073-449X. doi:10.1164/ajrccm.152.5.7582312. Consultado el 5 de noviembre de 2021.
- ↑ Di Stefano et al.: "Severity of airflow limitation is associated with severity of airway inflammation in smokers", en Am J Resp Crit Care Med, 158: págs. 1277-1285; 1998.
- ↑ Lim S. et al.: "Balance of matrix metalloproteasa-9 and tissue inhibitor of metalloprotease-1 from alveolar macrophagos in cigarretes smokers", en Am J Respir Crit Care Med 2000;162:1355-60
- ↑ O’Shaughenessy T. C. et al.: "Inflammation inbronchial biposies of subjects with chronic bronchitis:inverse relationship of CD8+ T lymphocyties with FEV1", en Am J Respir Crit Care Med, 155: págs. 852-857; 1997.
- ↑ Snider GL. et al. The definition of emphysema:report of National Heart,Lung and Blood Institute,Division of Lung Diseases, Workshop. Am Rev Respir Dis 1985; 132: 182-185.
- ↑ Myers, Allen R. (1997). Medicine (en inglés) (3ra edición). Lippincott Williams & Wilkins. pp. 71. ISBN 078172144X.
- ↑ Longmore, J. M.; Murray Longmore; Wilkinson, Ian; Supraj R. Rajagopalan (2004). Oxford handbook of clinical medicine. Oxford [Oxfordshire]: Oxford University Press. pp. 188-189. ISBN 0-19-852558-3.
- ↑ Myers, Allen R. (1997). Medicine (en inglés) (3ra edición). Lippincott Williams & Wilkins. pp. 66. ISBN 078172144X.
- ↑ «Global Initiative for Chronic Obstructive Lung Disease». Global Initiative for Chronic Obstructive Lung Disease - GOLD (en inglés estadounidense). Consultado el 4 de noviembre de 2021.
- ↑ Humanes, Vicent Carrascosa (20 de septiembre de 2023). «Rehabilitación pulmonar en EPOC: Beneficios y ejercicios». NEUMOFISIO. Consultado el 19 de febrero de 2024.
- ↑ Campbell Collaboration (2018). «Efectos positivos de la rehabilitación comunitaria para personas con discapacidades y sus cuidadores en países de ingresos medios y bajos». Oslo: Campbell Collaboration. Consultado el 3 de diciembre de 2019.
- ↑ Elsevier Article Locator
- ↑ Standards for the Diagnosis and Management of patients with COPD. American Thoracic Society y European Respiratory Society, 2004. American Thoracic Society y European Respiratory Society.
- ↑ «Calidad de vida en adultos mayores con enfermedad pulmonar obstructiva crónica».
- ↑ Young, R.P.; Hopkins, R; Eaton, T.E (2007). «Forced expiratory volume in one second: not just a lung function test but a marker of premature death from all causes». The European respiratory journal 30 (4): 616-622.
- ↑ a b c d Shirne, N; et al. (2023). «Multi-ancestry genome-wide association analyses improve resolution of genes and pathways influencing lung function and chronic obstructive pulmonary disease risk». Nature genetics 55 (3): 410-422.
- ↑ a b Sirugo, Giorgio; Williams, Scott M.; Tishkoff, Sarah A. (de marzo de 2019). «The Missing Diversity in Human Genetic Studies». Cell 177 (1): 26-31. doi:10.1016/j.cell.2019.02.048.
- ↑ a b Tobin, Martin D.; Izquierdo, Abril G. (de octubre de 2021). «Improving ethnic diversity in respiratory genomics research». European Respiratory Journal 58 (4): 2101615. doi:10.1183/13993003.01615-2021.
- ↑ a b Shirne, N; et al. (2019). «New genetic signals for lung function highlight pathways and chronic obstructive pulmonary disease associations across multiple ancestries». Nature genetics 51 (3): 481-493.
- ↑ Waine, L.V.; et al. (2017). «Genome-wide association analyses for lung function and chronic obstructive pulmonary disease identify new loci and potential druggable targets». Nature genetics 49 (3): 416-425.
- ↑ Mägi, R; et al. (2017). «Trans-ethnic meta-regression of genome-wide association studies accounting for ancestry increases power for discovery and improves fine-mapping resolution». Human molecular genetics 26 (18): 3639-3650.
Enlaces externos
[editar] Wikimedia Commons alberga una categoría multimedia sobre Enfermedad pulmonar obstructiva crónica.
Wikimedia Commons alberga una categoría multimedia sobre Enfermedad pulmonar obstructiva crónica.
- FORUMCLINIC Información sobre EPOC para pacientes en Español y Catalán: vídeos, noticias y foros
- Epocsite Información sobre EPOC para profesionales en Español: vídeos, noticias entrevistas con expertos, clases magistrales, publicaciones PubEpoc, cursos formativos, ponencias
- APEAS - Asociación de Pacientes de EPOC y Apnea del Sueño Archivado el 2 de febrero de 2017 en Wayback Machine.
- Global Initiative for Chronic Obstructive Lung Disease
- Fisterra Archivado el 31 de octubre de 2011 en Wayback Machine.
- Management of Stable Chronic Obstructive Pulmonary Disease: A Systematic Review for a Clinical Practice Guideline en Ann Intern Med
- HoNSelect
- EPOC en CDC
- Imágenes en MedlinePlus 19376
- Tutoriales Interactivos de Salud Medline Plus: Enfermedad pulmonar obstructiva crónica (EPOC) Utiliza gráficas animadas y se puede escuchar el tutorial
- Asociación Médica Argentina - Comité Antitabaco
- Tabaco y EPOC: una asociación comprobada

